Что такое дмпп сердца у ребенка. Дефект межжелудочковой перегородки у новорожденного: смертельный приговор или шанс на выздоровление
Дефект вторичной части межпредсердной перегородки может быть признаком ряда генетических заболеваний - синдрома Эллиса-Ван Кревельда, синдрома Нунан, синдрома Гольденхара, синдрома Кабуки, синдрома Вильямса и ряда хромосомных аномалий (трисомия 13, 18, 21-й пары, делеции хромосом 1, 4, 4p, 5p, 6, 10p, 11, 13, 17, 18, 22).
Некоторые заболевания матери (диабет, фенилкетонурия, острые лихорадочные болезни во время беременности), а также тератогенные воздействия на плод (антиконвульсанты, алкоголь, нестероидные противовоспалительные препараты) повышают риск возникновения ДМПП.
Причины дефекта перегородки:
В период эмбриогенеза межпредсердная перегородка закладывается из двух тканевых гребней. Один из них растет вверх от области первичного атриовентрикулярного соединения [согласно концепции Van Praagh и Сorsini - от участка левого венозного клапана (sinus venosus)] и называется первичной частью перегородки (septum primum) (нижняя треть перегородки). Он растет из задней части предсердия и затем встречается со вторичной частью перегородки. Вторичная часть (septum secundum) в виде гребня растет от основания сердца (верхней части предсердий) вниз. Между ними в средней трети перегородки находится овальная ямка, и в период внутриутробного развития в этой области функционирует овальное окно, которое является обязательным компонентом нормального внутриутробного кровообращения. Спонтанное закрытие овального окна происходит в первые недели либо месяцы жизни у большинства новорожденных, и обнаружение небольшого отверстия в области овальной ямки в этом возрасте не является основанием для постановки диагноза ДМПП.Дефекты предсердной перегородки представляют собой не закрывшиеся самостоятельно естественные отверстия МПП, возникшие в период закладки органов, либо как крайний вариант - полное недоразвитие одного из ее зачатков.
Типы межпредсердных дефектов:
Дефект вторичной части МПП составляет 80-90% всех ДМПП и локализуется в области овальной ямки либо верхней части перегородки, создавая шунт из левого предсердия в правое. Такой дефект возникает преимущественно из-за избыточной фенестрации или резорбции первичной части перегородки либо недоразвития вторичной части перегородки, а также при сочетании этих факторов. Примерно в 10% случаев ему сопутствует частичный аномальный дренаж легочных вен. ДМПП означает наличие истинной недостаточности ткани предсердной перегородки с сохранением функциональной и анатомической проходимости дефекта. Дефекты вторичной части предсердной перегородки часто называют вторичными ДМПП. Подобные дефекты не следует путать с незаращением овального отверстия. Анатомическая облитерация овального окна, как правило, следует за его функциональным закрытием вскоре после рождения.Дефект вторичной части перегородки может сочетаться с аневризмой МПП. Предположительно это является результатом избыточности ткани клапана овального окна. В таких случаях возможно сочетание с пролапсом митрального клапана и предсердными аритмиями.
К разновидностям дефекта вторичной части МПП также относятся редко встречающиеся дефекты: дефекты венозного синуса (unroofed coronary sinus), которые встречаются редко и составляют 3-4% всех ДМПП. Они располагаются в области соединения МПП с верхней полой веной и значительно реже - в месте впадения нижней полой вены в правое предсердие. При этих дефектах часть крыши коронарного синуса отсутствует, и поэтому кровь шунтируется из левого предсердия в коронарный синус и затем в правое предсердие. Дефекты венозного синуса, возникающие в верхней части МПП вблизи впадения верхней полой вены, нередко сопровождаются аномальным соединением легочных вен, исходящих из правого легкого с верхней полой веной и правым предсердием. Правые легочные вены могут аномально дренироваться в ПП, чаще у места впадения верхней полой вены (впадение правых легочных вен в нижнюю полую вену называется синдромом ятагана).
Дефект первичной части МПП, локализующийся в нижней ее трети. Аномалии типа первичного отверстия представляют собой разновидность дефекта развития эндокардиальных подушечек. Такие дефекты локализуются непосредственно рядом с атриовен-трикулярными клапанами, которые могут быть деформированы и некомпетентны в отношении выполнения своей функции, а иногда они образуют общий предсердно-желудочковый клапан.
Под термином «синдром Лютембаше» описывают редкую комбинацию ДМПП и стеноза левого атриовентрикулярного отверстия (митрального стеноза). Последний развивается как следствие приобретенного ревматического вальвулита.
В число регистрируемых ДМПП не входит открытое овальное окно (дефект в области овальной ямки размером до 0,2 см), которое встречается у 15-30% взрослых и не сопровождается расстройствами гемодинамики, по этой причине не требует лечения и не влияет на продолжительность жизни.
Гемодинамические расстройства
Объем шунтирования крови через межпредсердный дефект зависит от размера дефекта, сосудистого сопротивления в большом и малом круге кровообращения, податливости желудочков. В первые месяцы жизни левый и правый желудочки имеют одинаковую толщину стенки и поэтому одинаково растяжимы в диастоле, вследствие чего сброс слева направо невелик. Позже податливость ПЖ возрастает по мере снижения постнагрузки на него из-за уменьшения легочного сосудистого сопротивления, сброс слева направо через шунт увеличивается и возникает дилатация ПП и ПЖ. Величина сброса крови слева направо через ДМПП зависит от размеров дефекта, относительной податливости желудочков и величин сосудистого сопротивления легочного и системного круга кровообращения.
При небольшом ДМПП давление в левом предсердии превышает давление в правом на несколько миллиметров ртутного столба, тогда как при большом межпредсердном дефекте давления в предсердиях могут стать равными. Шунт крови слева направо приводит к диастолической перегрузке правого желудочка и повышению легочного кровотока. Сопротивление сосудов легких у детей с ДМПП обычно нормальное или понижено, а объемная нагрузка хорошо переносится, хотя легочный кровоток может превышать системный в 3-6 раз. Тем не менее у большинства детей с вторичным ДМПП нет никаких субъективных симптомов. Гиперволемия приводит к легочной гипертензии, но она в течение длительного времени выражена умеренно, а необратимые (обструктивные) изменения легочных сосудов при этом пороке формируются обычно не ранее 2-3-го десятилетия жизни. Во время беременности в связи с возрастанием общего объема плазмы объем шунта на уровне предсердий может значительно увеличиться.
Срок появления симптомов:
Хотя порок существует с рождения, шум появляется спустя несколько месяцев либо не выслушивается совсем. В связи с частым отсутствием шума в сердце и симптомов застойной сердечной недостаточности порок обычно распознают при скрининговых эхокардиографических исследованиях, реже - по транзиторному дистальному цианозу и иногда по парадоксальным тромбоэмболиям.Симптомы дефекта межпредсердной перегородки:
Клиническая картина зависит от возраста больного, размеров дефекта, величины сосудистого сопротивления легких. Большинство пациентов с этим пороком выглядят здоровыми, и родители не предъявляют никаких жалоб. Признаками умеренного сброса крови слева направо могут быть непереносимость повышенной физической нагрузки и утомляемость. В большинстве случаев при аускультации нет шума в сердце, иногда даже при большом ДМПП, поскольку разница давлений между левым и правым предсердием невелика и небольшой градиент на участке сброса не создает слышимого звука. I тон обычно нормальный, иногда может быть расщеплен. Значительное увеличение объема крови, текущей через клапан легочного ствола, приводит к возникновению среднесистолического шума изгнания (так называемому гемодинами-ческому стенозу легочной артерии) во втором и третьем межреберьях слева от грудины. Обычно выслушивается отчетливое и не связанное с дыханием расщепление II тона либо усиление II тона над легочной артерией. Симптомов застойной СН чаще нет, либо они выражены умеренно.При межпредсердном дефекте часто встречается пролапс митрального клапана. Причиной этого может быть компрессия левых отделов сердца из-за увеличения правых. У таких пациентов с ПМК выслушивается голосистолический либо позднесистолический шум на верхушке, часто иррадиирующий в аксиллярную область; может быть слышен среднесистолический клик.
Иногда при очень больших размерах дефекта наблюдаются одышка, тахикардия, гепатомегалия, может появиться сердечный горб, границы сердца расширены вправо, усилена пульсация ПЖ желудочка и может пальпаторно определяться пульсация легочной артерии. В этих случаях не только ПЖ, но и легочная артерия значительно дилатированы, поэтому гемодинамический стеноз клапана ЛА сменяется его недостаточностью и появляется диастолический шум Грэхема-Стилла (шум относительной гемодинамической недостаточности клапана легочной артерии во втором и третьем межреберьях слева от грудины).
У пациентов с общим предсердием наблюдается право-левое шунтирование и цианоз, хотя он обычно выражен слабо.
Тяжелая сердечная недостаточность редко развивается при вторичном ДМПП, лишь у 3-5% больных, и только при очень большом размере дефекта, особенно если это дефект типа венозного синуса (sinus venosus). В этой небольшой группе больных серьезная СН и задержка физического развития возникают в возрасте до 1 года (в половине этих случаев из-за гемодинамических расстройств и еще в половине - из-за сочетанной органной недостаточности вследствие сопутствующих пороков развития). В этой маленькой группе летальность достигает 10%, если не выполнена операция.
Очень редко первым симптомом межпредсердного дефекта бывает эмболический инсульт.
При нераспознанном ДМПП симптомы сердечной недостаточности могут впервые появиться во время беременности в связи с возрастанием объема циркулирующей крови.
Диагностика
На фронтальной рентгенограмме грудной клетки при небольших и средних размерах дефекта изменений может не быть. При больших дефектах возникает усиление легочного рисунка, расширение границ сердечной тени из-за дилатации ПП, ПЖ; легочная артерия расширена и выбухает слева между контуром аорты и ЛЖ.
На электрокардиограмме при небольших дефектах нет изменений. При дефекте большого размера электрическая ось имеет вертикальное положение или отклонена вправо (+95 ... +170?). Если объем шунтирования слева направо составляет более 50% минутного объема малого круга кровообращения, появляются признаки гипертрофии ПЖ и ПП (rsR морфология в V1, подчеркнутый S-зубец в левых грудных отведениях, отсутствие зубца Q в левых грудных отведениях, остроконечный Р-зубец). При любом типе дефекта, особенно при дефекте венозного синуса, может быть удлинен интервал P-R. У более старших детей появляются предсердные аритмии (наджелудочковая экстраси-столия и тахикардия, трепетание предсердий).
Лабораторные данные - общий анализ крови и газовый состав крови в норме.
При допплерэхокардиографии определяются локализация и размер дефекта, направление сброса крови через него, дилатация ПП и ПЖ, ствола ЛА.
Дополнительно при большом дефекте МПП определяются парадоксальное движение МЖП, признаки трикуспидальной регургитации II-III степени, повышение давления в правом желудочке и легочной артерии. При чреспищеводной эхокардиографии могут быть выявлены аномалии легочных вен, ассоциированных с межпредсердным дефектом типа situs venosus.
Катетеризация сердца и ангиокардиография:
Требуется очень редко, в тех случаях, когда наблюдается несоответствие клинических симптомов порока данным инструментальных исследований. В основном применяется с целью оценки степени легочной гипертензии, если она выражена, наличия легочно-системного шунтирования и оценки резистентности легочного сосудистого русла.Естественная эволюция порока
Без оперативного лечения легочная гипертензия прогрессирует, но появление обструктивного поражения сосудов легких (ЛГ III-IV степени) наблюдается со 2-3-го десятилетия жизни, т.е. позже, чем при ДМЖП и ОАП. При нераспознанном межпредсердном дефекте у подростков и взрослых присоединение артериальной гипертензии увеличивает объем лево-правого сброса. В поздней стадии порока происходит значительный рост резистентности сосудов малого круга, что в подростковом возрасте либо после 18 лет приведет к обструктивному поражению сосудов легких и снижению степени лево-правого шунта.Кроме того, из-за дилатации ПП возникают стойкие предсердные аритмии (в том числе мерцательная аритмия). Вследствие серьезной дилатации ПП пациентам угрожают тромбоэмболические осложнения (в первую очередь инсульт). Перечисленные причины ограничивают качество и продолжительность жизни. Правожелудочковая застойная сердечная недостаточность при больших размерах дефекта усиливается во время беременности и может привести к неблагоприятному исходу.
Примерно у 15% больных с дефектами вторичной части перегородки небольшого или среднего размера эти дефекты могут закрыться спонтанно к 4-5 годам жизни либо уменьшиться в размерах настолько, что становятся гемодинамически незначимыми.
Наблюдение до операции
При признаках СН и ЛГ назначаются диуретики и ингибиторы АПФ, при необходимости также дигоксин.
Сроки оперативного лечения:
Показаниями к операции в возрасте до 1 года являются симптомы серьезной сердечной недостаточности и задержка физического развития. Для остальных пациентов оптимальный возраст операции - 2-3 года, даже если симптомов нет или они минимальны.Виды оперативного лечения:
Первую успешную операцию ушивания вторичного ДМПП выполнил 2 сентября 1952 г. хирург F. Lewis в клинике медицинского университета штата Миннесота (США) у 5-летней девочки с большим межпредсердным дефектом в условиях общей гипотермии с периодом пережатия аорты менее 6 мин. Ребенок выздоровел без осложнений и без применения современных методов послеоперационной интенсивной терапии и был выписан из госпиталя через 11 дней. Именно по поводу ДМПП проведена первая в мире операция с использованием искусственного кровообращения, когда врач J. Gibbon 6 мая 1953 г. применил созданный им насосный оксигенатор при закрытии ДМПП.В зависимости от размеров и морфологического типа дефекта в настоящее время применяются следующие операционные методики.
Ушивание либо пластика дефекта в условиях искусственного кровообращения из доступа методом срединной стернотомии либо из правосторонней передней торакотомии.
Окклюзия устройством Амплатцера при правильной форме дефекта и наличии у него окружающего края не менее 0,5 см. Попытки кате-терной окклюзии межпредсердного дефекта начались с 1950-х гг., когда различными устройствами пробовали закрыть дефект без применения искусственного кровообращения. В середине 1970-х гг. доктора Т. King и N Mills запатентовали открытое ими устройство, которое позволяет лечить ДМПП с помощью мини-инвазивной транскатетерной манипуляции без операции с искусственным кровообращением. Т. King также впервые произвел эту манипуляцию при межпредсердном дефекте. В течение последних двух десятилетий произошли значительные изменения в подходах к лечению этого порока - внедрено транскатетерное закрытие вторичного межпредсердного дефекта у значительной части взрослых пациентов и детей. За прошедшие более чем 30 лет были испытаны многие разновидности окклюзирующих устройств. Окклюдер для закрытия ДМПП изготавливается в настоящее время в виде одиночного либо двойного диска из различных материалов и с разными видами катетеров, доставляющих устройство в сердце через магистральные вены.
Транскатетерное закрытие ДМПП во вторичной части применяется в мире и у маленьких детей массой менее 10 кг. Недавно в США началось применение биоабсорбирующих-ся окклюдеров у пациентов в возрасте 2,5-13 лет с хорошим результатом на протяжении 6-12 мес наблюдения. Эти окклюдеры (BioSTAR) относятся к биоинженерным устройствам - они изготовлены из высоко-очищенного ацеллюлярного матрикса, содержащего в своей основе на-тивный интерстициальный коллаген. Технические правила установки и последующего наблюдения биодеградирующих окклюдеров идентичны таковым при установке обычных окклюдеров Амплатцера, за исключением последующей постепенной биодеградации устройства с заменой собственной фиброзной тканью.
При кажущейся простоте этой процедуры существует ряд факторов, влияющих как на возможность, так и на успех ее выполнения. К ним относятся морфологические особенности дефекта, наличие сопутствующих заболеваний, а также ряд индивидуальных признаков, таких как возраст, рост, масса тела. Осложнения встречаются менее чем у 1% больных, к ним относятся перфорация стенки сосуда, сосудистые тромбозы, смещение окклюдером.
Дилатация ПЖ регрессирует с примерно одинаковой скоростью при обеих хирургических техниках. Время пребывания в больнице заметно меньше при транскатетерной процедуре, и реабилитация после выписки короче.
Результат оперативного лечения:
Ранняя операция наиболее эффективна, а при поздно выполненной могут длительно сохраняться уже возникшие до операции легочная ги-пертензия, дилатация правого предсердия и предсердные аритмии.При открытой операции (с искусственным кровообращением) хирургическая летальность не более 0,1%. Осложнения (СССУ, АВ-бло-када) встречаются редко.
При катетерной окклюзии дефекта устройством Амплатцера осложнения встречаются у 3-4% пациентов (эмболии, перфорация стенки сосудов либо сердца, тампонада сердца, аритмии, окклюзии сосудов, неполное закрытие дефекта, резидуальный шунт, неправильное положение устройства со смещением атриовентрикулярных клапанов). Летальность вследствие указанных осложнений менее 1%.
Особенности закрытия ДМПП у детей раннего возраста:
При изолированном ДМПП у пациентов нередко нет клинических симптомов в младенческом возрасте и раннем детстве, поэтому оперативное вмешательство обычно может быть отложено до возраста 2- 4 лет. Однако хорошо известно, что существует небольшая часть детей младшего возраста с ДМПП, требующих более ранней хирургической интервенции, если порок сочетается с хроническими заболеваниями легких либо некоторыми хромосомными аномалиями.В последние годы появляется все больше сообщений об успешном результате транскатетерного закрытия ДМПП даже у детей с массой тела менее 10 кг, с низким числом осложнений. Тем не менее следует помнить, что узкий просвет сосудов, через которые проводится сравнительно ригидный проводник, несущий устройство Амплатцера, влечет за собой более значимый риск сосудистого повреждения, чем у старших детей. Младенцы также имеют более высокий риск повреждения сердца при данной манипуляции. Наследственный тип ДМПП обычно сопровождается относительно малой шириной предсердного края вокруг дефекта, что может помешать установке окклюдера с маленькими дисками либо приведет к эрозии перегородки или необходимости прекращения процедуры.
Из-за маленького размера перегородки попытка установки окклюде-ра может быть неудачной и в связи с дефицитом ткани по краю дефекта, необходимой для фиксации устройства около митрального клапана. Таким образом, чтобы убедиться в безопасности транскатетерной окклюзии, необходимо тщательно оценить все указанные факторы и желательно также обладать опытом выполнения подобных процедур у младенцев. Для больных раннего возраста предложена в настоящее время индивидуальная техника подбора левопредсердного диска.
Дефект межпредсердной перегородки у детей - это группа врожденных пороков сердца, для которых характерно наличие аномального сообщения между двумя предсердными камерами. Дефекты межпредсердной перегородки у детей различаются по расположению отверстия. Часто встречаются центральный, верхний, нижний, задний, передний дефекты. Также дефект может квалифицироваться по его размеру от небольшого щелевидного отверстия, например, при незаращении овального окна, до полного отсутствия овального окна. Встречается также и полное отсутствие межпредсердной перегородки - единственное предсердие. Решающее значение для диагностики и дальнейшего лечения имеет количество дефектов (от одного до многих). Неодинаково располагаются дефекты и в отношении места впадения верхней и нижней полых вен.
Как проявляется дефект межпредсердной перегородки у детей
Клинически и симптоматически обычно проявляются только дефекты межпредсердной перегородки с величиной в 1 см и более. В результате наличия межпредсердного сообщения происходит смешивание крови в предсердиях. Кровь течет из предсердия с большим систолическим давлением (слева) в предсердие с меньшим давлением (справа). Уровень давления имеет значение в определении направления сброса крови лишь в тех случаях, когда диаметр дефекта не превышает 3 см.
При больших дефектах межпредсердной перегородки у детей компонент давления отсутствует, однако сброс крови, как правило, идет слева направо, поскольку ток крови из правого предсердия в правый желудочек встречает при движении значительно меньшее сопротивление, чем ток крови из левого предсердия в левый желудочек. Это обусловлено анатомическими особенностями правого предсердия: тонкая и более податливая к растяжению стенка предсердия и желудочка; большая площадь правого атриовентрикулярного отверстия по сравнению с левым (10,5 и 7 см), большая лабильность и емкость сосудов малого круга кровообращения.
В результате сброса крови через дефект из левого предсердия в правое развивается увеличение наполняемости кровью малого круга кровообращения, увеличивается объем правого предсердия и усиливается работа правого желудочка. Повышение давления в легочной артерии развивается в 27% случаев и наблюдается в основном у детей старшего возраста. В результате увеличения объема крови наблюдается расширение легочного ствола и левого предсердия. Левый желудочек остается нормальным по размеру, а при большом объеме дефекта межпредсердной перегородки может быть даже меньших размеров, чем в норме.
У новорожденных детей вследствие высокого легочно-капиллярного сопротивления и низкого давления в левом предсердии может периодически наблюдаться сброс крови из правого предсердия в левое отделение. У детей раннего возраста также может легко изменяться направление движения крови в связи с повышением давления в правом предсердии (при большой физической нагрузке, заболеваниях органов дыхания, крика, сосании). В поздних стадиях болезни при увеличении давления в правых камерах сердца, вследствие развития гипертензии в малом круге кровообращения возникает перекрестный сброс, а затем постоянный сброс венозной крови из правого предсердия в левое отделение.
Врожденный дефект межпредсердной перегородки и его клиника
Клиника врожденного дефекта межпредсердной перегородки отличается большим разнообразием. В течение первого месяца жизни основным, а нередко и единственным симптомом является непостоянный, слабо выраженный цианоз, что проявляется при крике, беспокойстве, который у ряда детей остается незамеченным.
Основные симптомы пороков начинают проявляться на 3-4 месяцах жизни, однако часто диагноз пороков ставится только в 2-3 года и даже позже.
При небольших дефектах межпредсердных перегородок (до 10-15 мм) дети физически развиты нормально, жалобы отсутствуют.
В раннем детстве у детей с большим дефектом межпредсердной перегородки наблюдается отставание в физическом развитии, психическом развитии, развивается недостаточность веса. Они часто болеют респираторными заболеваниями. Признаки застойной недостаточности у них, как правило, отсутствуют. В старшем возрасте у детей также наблюдается отставание в росте, опоздание полового развития, в то же время физические нагрузки они переносят плохо.
При осмотре кожа бледная. Деформация грудной клетки в виде центрального сердечного горба, которая обусловлена ослабеванием мышечного тонуса и увеличением в размерах правого желудочка, отмечается в 5-3% случаев (при больших дефектах и быстро прогрессирующей легочной гипертензии у детей немного старшего возраста). Систолическое дрожание, как правило, отсутствует. Верхушечный толчок средней (нормальной) силы или усилен, смещен влево, всегда разлит, обусловленный гипертрофированным правым желудочком.
Границы сердца расширены вправо и вверх, главным образом за счет увеличения правого предсердия и легочного ствола, но при больших дефектах и у детей старшего возраста отмечается также расширение отделов сердца, как правило, за счет правого желудочка, что оттесняет левый желудочек назад. Выраженные симптомы расширения сердечных границ встречаются редко.
Пульс нормального напряжения и несколько сниженного наполнения. Артериальное давление в норме или снижено систолическое и пульсовое артериальное давление при большом шунте крови через дефект.
При прослушивании: тон чаще усиленный из-за уменьшения загруженности левого желудочка и усиленного сокращения перегруженного объемом правого желудочка, II тон, как правило, усилен и расщеплен над легочной артерией из-за увеличения объема крови и повышения давления в малом круге кровообращения и позднего закрытия пульмонального клапана, особенно у детей старшего возраста. Систолический шум - средней интенсивности и продолжительности, не грубого тембра - выслушивается локально в 2-3-м межреберье слева от грудины, умеренно проводится к левой ключице и реже до 5 точки Боткина. Шум лучше выслушивается в положении больного лежа, на глубине максимального выдоха. При физической нагрузке шум при дефекте межпредсердной перегородки усиливается, в отличие от физиологического шума (умеренного акцента тона над легочной артерией у здоровых детей до 10-летнего возраста), который при нагрузке исчезает. Кроме основного систолического шума, у детей старшего возраста может выслушиваться короткий междудиастолический шум относительного стеноза трикуспидального клапана (шум Кумбса), связанный с увеличением кровообращения через правое атриовентрикулярное отверстие.
В поздних стадиях заболевания, при значительном расширении ствола легочной артерии (у 10-15% больных) иногда появляется нежный протодиастолический шум относительной недостаточности пульмонального клапана.
Диагноз изолированного вторичного дефекта межпредсердной перегородки у детей ставят на основе следующих признаков - появление неинтенсивного транзиторного цианоза в течение первых 2-3 месяцев жизни, частые респираторные заболевания на первом году жизни, выслушивание умеренного систолического шума в 2 межреберье слева от грудины.
Со второго полугодия или после года - наличие признаков перегрузки правого предсердия, гипертрофии правого желудочка, интактный левый желудочек по данным ЭКГ, Эхо-КГ, катетеризации полостей сердца, признаков перегрузки малого круга кровообращения.
Дифференциальный диагноз проводится с функциональным систолическим шумом, врожденными пороками сердца (открытый аортальный порок сердца, дефект межжелудочковой перегородки, стеноз устья аорты), недостаточностью митрального клапана.
Осложнения и прогноз межпредсердной перегородки у детей
В числе осложнений дефекта межпредсердной перегородки сердца у детей наиболее часто встречается ревматизм и бактериальная вторичная пневмония. Присоединение ревматизма наблюдается у 10% пациентов, в основном заканчивается летально либо образуются митральные пороки.
Аритмии возникают в результате резкой дилатации правого предсердия (экстрасистолия, пароксизмальная тахикардия, мерцательная аритмия и другие нарушения ритма).
В результате частых респираторных заболеваний, пневмоний у ряда больных формируется хронический неспецифический бронхолегочный процесс.
Легочная гипертензия развивается в возрасте 30-40 лет и старше.
Средняя продолжительность жизни при вторичном дефекте межжелудочковой перегородки сердца у детей - 36-40 лет, однако некоторые пациенты доживают до 70 лет, но после 50 лет становятся инвалидами. Спонтанное закрытие дефекта межжелудочковой перегородки у детей наступает в 5-6 лет в 3-5%.
Иногда дети с дефектом межжелудочковой перегородки погибают в грудном возрасте в результате тяжелой недостаточности кровообращения или пневмоний.
Лечение дефекта межпредсердной перегородки у детей
Лечение дефекта межпредсердной перегородки у детей подразделяется на хирургическое и консервативное. Последнее направлено в основном на устранение последствий недостаточности кровообращения.
Оптимальным сроком оперативного закрытия дефекта является возраст 5-6 лет. Показания к операции: выраженные нарушения гемодинамики в системе малого круга кровообращения.
Операция выполняется на сухом сердце в условиях гипотермии и искусственного кровообращения. Небольшие вторичные дефекты межпредсердной перегородки у детей закрывают ушиванием. При больших дефектах, первичных дефектах межпредсердной перегородки у детей из-за опасности прорезывания швов дефект всегда закрывается с помощью метода пересадки тканей. Летальность не превышает 2%. Летальность тем выше, чем выше степень легочной гипертензии, недостаточности кровообращения и нарушение сердечного ритма и проводимости, наличие тяжелых проявлений эндогенного эндокардита.
Частые причины летальных исходов: острая сердечная недостаточность, эмболия и кислородное голодание головного мозга.
pediatriya.info
Симптомы ДМПП
У новорожденных ДМПП никак не проявляется, поэтому порок часто обнаруживается либо при плановой диагностике, либо при появлении специфических симптомов. ДМПП характеризуется:
- шумами в сердце (обнаруживаются через аускультацию);
- одышкой при выполнении упражнениях разной тяжести;
- постоянной усталостью и вялостью;
- отеками нижних и верхних конечностей, живота;
- учащенным сердцебиением, которое ощущается в состоянии покоя;
- частыми осложнениями ОРЗ (легкие).
Внимание: если у вашего ребенка обнаружен хотя бы один из вышеуказанных симптомов, необходимо срочно отправиться к врачу на прием. Потому как одышка, утомляемость, отеки и ускоренное сердцебиение свидетельствуют в первую очередь о наличии осложнения ДТПП (сердечной недостаточности и других характерных заболеваний).
Причины ДМПП у детей
До этого момента точные причины формирования порока сердца, в том числе ДМПП, не установлены. Если говорить о механизме возникновения патологий, то все они являются следствием нарушений развития плода на ранних этапах. Причинами называются генетические сбои и экологические факторы.
Врачи акцентируют внимание на том, что, ДМПП и другие патологии возникают как следствие негативного влияния внешнего или внутреннего характера. Течение ДМПП у детей обусловлено тем, что миокард левых отделов испытывает нагрузку меньше, чем правые, соответственно, обогащенная кровь в правом предсердии смешивается с кровью, которая практически не содержит кислорода. Поскольку она затем снова попадает в легкие, возникает перегрузка, от которой страдают правые отделы сердечной мышцы и легкие.
Со временем из-за постоянных и значительных нагрузок, правые отделы расширяются, возникает гипертрофия, а это приводит к ослаблению сердечной мышцы, о котором мы упоминали выше. Одним из осложнений на данном этапе ДМПП может стать застой жидкости в легочном круге кровообращения.
Видео — ДМПП или дефект межпредсердной перегородки
ДМПП и незаращение овального окна: различаем патологии
Когда мы говорим о ДМПП, подразумеваем наличие отверстия между правым и левым предсердием, которое анатомически не заложено; овальное окно, наоборот, является естественным отверстием, предназначающимся для осуществления кровотока плода в утробе матери. После появления ребенка на свет, овальное окно должно зарасти. Если этого не случилось, мы говорим о малой патологии (МАРС-синдром), проявления которой напрямую зависят от размеров окна. К тому же окно может закрыться на протяжении первых пяти лет жизни.
Факторы риска развития ДМПП
Как мы уже говорили ранее, врачи не могут назвать точных причин формирования пороков сердца. Однако исследования продолжают проводиться и медикам удалось обозначить факторы риска, которые при определенных условиях приводят к возникновению патологии.
Во-первых, это генетическая предрасположенность, если у кого-то из родственников поставили диагноз ДМПП, значит, у вас отягощенная наследственность. Желательно пройти консультацию у врача генетика, чтобы узнать риск возникновения этого заболевания у будущего ребенка.
Во-вторых, факторами риска являются болезни, которыми женщина переболела в процессе вынашивания плода. Например, краснуха — вирусное заболевание, особенно опасное для плода на ранних сроках беременности.
Именно в этот период формируются основные органы и возможны аномалии, например, ДМПП.
В-третьих, на развитии ребенка в утробе матери может сказаться прием некоторых медикаментозных препаратов, курение, употреблением алкоголя и плохая экологическая ситуация, стрессы, неправильное питание.
Основные осложнения ДМПП
Если отверстие маленькое, ребенок может не ощущать дискомфорта, к тому же небольшие дефекты могут закрыться сами в первые года жизни. Но если речь идет о значительном отверстии, то вскоре появляются первые осложнения. Чаще всего больным ДМПП ставят диагноз легочной гипертензии (из-за чрезмерной нагрузки правые отделы растягиваются, ослабевают и увеличиваются в размерах), возникают застойные явления.
В исключительных случаях гипертензия способствует развитию синдрома Эйзенменгера (необратимые изменения в легких).
Среди осложнений встречается аритмия, при длительном отсутствии лечения развивается сердечная недостаточность.
Диагностика сердечных патологий
Дефект перегородки можно обнаружить и в процессе планового медосмотра. Как правило, первые подозрения на ДМПП возникают после проведения аускультации (слышны шумы в сердце). Дает возможность обнаружить патологию и УЗИ сердца (эхокардиограмма).
Если ваш лечащий врач подозревает вышеуказанное отклонение в функционировании сердца, чтобы подтвердить диагноз понадобятся специфические методы исследования:
- уже указанная выше эхокардиограмма (оценивает работу сердечной мышцы и ее состояние);
- рентгенография грудной клетки (дает возможность обнаружить расширение отдельных отделов. Если на снимке видно расширение правых отделов, скорее всего, у пациента присутствует патология ДМПП);
- пульсоксиметрия (метод изучения крови на предмет содержания кислорода. Процедура абсолютно безболезненна для ребенка, выполняется с помощью датчика, он и подсчитывает количество кислорода);
- катетеризация сердца (через артерию с помощью катетера в систему кровотока впрыскивается контрастное вещество, с помощью снимков фиксируется его путь. Это позволяет сделать выводы о функциональном состоянии сердца и выявить патологию);
- МРТ(магнитно-резонансная томография) дает возможность оценить состояние структурных элементов сердца, не подвергая ребенка рентгеновскому излучению. Обычно, МРТ используют как дополнительный метод постановления диагноза, если результаты предыдущих исследований не дали однозначного ответа о наличии патологии.
Лечение ДМПП у детей
Детям с отверстием в межпредсердной перегородке нужно оперативное хирургическое вмешательство. Если отверстие небольшое, врач может принять решение какое-то время понаблюдать за состоянием ребенка. Бывает, что патология не наносит ощутимого вреда и сердце функционирует нормально. Но в большинстве случаев, наличие отверстия несет прямую угрозу жизни и операции не избежать. Риски хирургического вмешательства зависят от состояния здоровья пациента, присутствия функциональных патологий, состояния сердечной мышцы.
Медикаментозная поддержка
Ни один существующий препарат не может стимулировать устранение патологии.
Консервативное лечение направлено прежде всего на то, чтобы уменьшить негативные влияния порока и устранить риск ухудшения состояния. Больным назначают препараты, способные регулировать ритм сердца, а также антикоагулянты, чтобы предупредить образование тромбов. Медикаментозная терапия проводится также перед операцией, чтобы скорректировать состояние больного.
Оперативное вмешательство
Желательно провести операцию по устранению ДМПП сразу после его обнаружения, когда организм еще не так сильно пострадал от патологии. Операция предусматривает закрытие отверстия с помощью «заплатки» или его сшивание. Благодаря этому, удается предотвратить смешение жидкости в правом предсердии. Операция проводится путем катетеризации или на открытом сердце (пациента подключают к аппарату искусственного кровообращения и вшивают заплатку на основе синтетических не аллергенных материалов). Второй вариант операционного вмешательства опаснее из-за риска возникновения осложнений.
Эндоваскулярное закрытие патологии
Поскольку операции на открытом сердце очень опасны, требуют подключения больного к аппаратам поддержания жизни и чреваты последствиями или, как минимум, длительной реабилитацией, медики активно искали менее опасный и травматичный метод устранения пороков сердца. Когда речь идет оДМПП, операция проводится с помощью окклюдера. Это аппарат, который в сложенном виде помещается в тонкую трубку катетера и вводится пациенту. Визуально окклюдер похож на два диска, обладает эффектом памяти формы. Окклюдеры создаются из нитинола, полностью биосовместимые, не вызывают аллергии и не обладают магнитными свойствами.
Перед операцией пациент должен пройти процедуру ультразвукового исследования сердца (транспищеводную), благодаря ей врачи получают точную информацию об особенностях строения органа и анатомии порока.
Этот метод исследования позволяет определить показания и противопоказания такого типа лечения. Несмотря на то, что эндоваскулярная операция не требует надрезов, большинству пациентов процедуру делают под наркозом (датчик вызывает дискомфорт). Информацию о размере дефекта измеряют через ЭхоКГ, затем через бедренную вену водят окклюдер (в сложенном виде) и устанавливают так, чтобы диски находились в правом и левом предсердии. Если операция успешна, заплатка закрывает просвет и кровь больше не смешивается.
Если окклюдер сместился, его втягивают в катетер и процесс повторяется. После того как заплатка установлена, аппарат извлекается наружу. Процедура занимает не более часа (с подготовкой пациента). Еще сутки пациент должен пребывать под наблюдением врачей и пройти обследование.
По статистике приблизительно 90% больных с дефектом межпредсердной перегородки могут пройти лечение таким образом. Противопоказаниями к процедуре являются дефекты без краев, а также наличие некоторых сердечно-сосудистых аномалий (принимать решение о возможности проведения эндоваскулярной операции должен врач).
Реабилитационный курс, как правило, занимает шесть месяцев. В это время пациенту стоит воздержаться от физических нагрузок, вакцинации и беременности. А также принимать ряд препаратов по предписанию доктора.
Операция на открытом сердце
Если размер дефекта не превышает 1,2 (по некоторым данным до 3) сантиметра, его ушивают. Если отверстие больше, то оно закрывается с помощью заплатки. Второй вариант устранения патологии предпочтительнее, потому что он в меньшей степени способствует образованию тромбов на месте хирургического вмешательства.
В дальнейшем пациент должен регулярно наблюдаться у кардиохирурга, восстановительная терапия длится год. Только по прошествии этого времени больному разрешается физическая активность.
Видео — Пластика дефекта межпредсердной перегородки
Прогноз
Прогноз зависит прежде всего от того, когда была проведена операция. Если дефект был устранен в детстве или юности, есть хорошие шансы, что осложнений удастся избежать. Имеет значение и функциональное состояние сердечной мышцы: насколько на ее работу повлияла патология и какой ущерб нанесен. Чаще других среди постоперационных осложнений встречается аритмия. Если на момент операции у ребенка развилась сердечная недостаточность, устранить заболевание, увы, невозможно даже с помощью операции. В таком случае хирургическое вмешательство нужно прежде всего для того, чтобы не допустить ухудшения состояния больного. При своевременном лечении ребенок может полностью излечиться от ДМПП.
med-explorer.ru
Диагностика дефекта межпредсердной перегородки
Диагноз предполагают на основании данных физикального обследования сердца, рентгенографии органов грудной клетки и ЭКГ, подтверждают при эхокардиографии с помощью цветной допплеркардиографии.
Катетеризация сердца обычно не требуется, если только не подозревают наличие сочетанных пороков сердца.
При клиническом осмотре сердечный горб обнаруживают в более старшем возрасте у детей с кардиомегалией, систолическое дрожание выявляют редко, его наличие свидетельствует о возможности сопутствующего порока (стеноз лёгочной артерии, дефект межжелудочковой перегородки). Верхушечный толчок ослабленный, неразлитой. Границы относительной сердечной тупости могут быть расширены в обе стороны, но за счёт правых отделов: левая граница — из-за смещения влево увеличенным правым желудочком левого, правая граница — за счёт правого предсердия.
Основной аускультативный признак, позволяющий заподозрить дефект межпредсердной перегородки, -систолический шум средней интенсивности, негрубый, без выраженной проводимости, с локализацией во втором-третьем межреберье слева у грудины, лучше выслушиваемый в ортостазе. Мнение о происхождении систолического шума едино: он связан с функциональным стенозом лёгочной артерии, возникающим из-за увеличения кровотока при неизменённом фиброзном кольце лёгочного клапана. По мере повышения давления в лёгочной артерии появляется и нарастает акцент II тона над лёгочной артерией.
С развитием относительной недостаточности трикуспидального клапана нарастает перегрузка предсердий, возможно появление нарушений сердечного ритма. На ЭКГ характерно отклонение электрической оси сердца вправо до +90…+120. Признаки перегрузки правого желудочка имеют неспецифический характер: неполная блокада правой ножки пуска Гиса в виде rSR в отведении V1. По мере увеличения давления в лёгочной артерии и перегрузки правого желудочка амплитуда зубца R нарастает. Обнаруживают и признаки перегрузки правого предсердия.
Данный порок не имеет специфических рентгенологических признаков. Выявляют усиление лёгочного рисунка. Изменение размеров сердца на рентгенограмме определяется величиной сброса. В косых проекциях видно, что сердце увеличено за счёт правых камер. При рентгенографии органов грудной клетки обнаруживают кардиомегалию с дилатацией правого предсердия и правого желудочка, расширение тени легочной артерии и усиление легочного рисунка.
Трансторакальная двухмерная ЭхоКГ позволяет непосредственно обнаружить перерыв эхосигнала в зоне межпредсердной перегородки. Диаметр дефекта межпредсердной перегородки, определённый эхокардиографически, практически всегда отличается от измеренного во время операции, что связано с растяжением сердца движущейся кровью (в период операции сердце расслаблено и опорожнено). Именно поэтому измерение фиксированных тканевых структур возможно произвести довольно точно, а меняющихся параметров (диаметр отверстия или полости) — всегда с определённой ошибкой.
Катетеризация сердца и ангиокардиография в настоящее время потеряли свое значение в диагностике дефекта межпредсердной перегородки. Применение данных методов целесообразно лишь при необходимости точного измерения величины сброса через дефект или степени лёгочной гипертензии (у пациентов старших возрастных групп), а также дли диагностики сопутствующей патологии (например, аномального дренажа лёгочных вен).
Дифференциальная диагностика дефекта межпредсердной перегородки
Дифференциальную диагностику при вторичном дефекте межпредсердной перегородки прежде всего проводят с функциональным систолическим шумом, выслушиваемым на основании сердца. Последний ослабевает в положении стоя, правые отделы сердца не увеличены, неполная блокада правой ножки пучка Гиса не характерна. Достаточно часто дефект межпредсердной перегородки приходится дифференцировать с такими заболеваниями, как изолированный стеноз лёгочной артерии, триада Фалло, аномальный дренаж лёгочных вен, дефект межжелудочковой перегородки, аномалия развития трёхстворчатого клапана (аномалия Эбштейна).
ilive.com.ua
Симптоматика
У новорожденных чаще всего не обнаруживается какой-либо симптоматики этого вида ВПС. Признаки дефекта в большинстве случаев начинают обнаруживаться к 30-летнему возрасту или даже позднее. Данная разновидность порока чаще встречается у женщин.
Проявления ДМПП:
- шумы в сердце;
- быстрое уставание;
- диспноэ (в первую очередь при физических нагрузках);
- отечность в области ног, стоп и живота;
- учащенный сердечный ритм;
- регулярные рецидивы инфекционных болезней легких;
- острое нарушение мозгового кровообращения;
- синюшность кожи.
Однозначного мнения о причинах развития пороков сердца не существует. ВПС, в частности, дефект межпредсердной перегородки, возникает как результат неправильного развития сердца на начальных стадиях формирования плода. Существенное влияние на процесс оказывают генетика и экология.
Основными факторами риска, способными повлиять на развитие дефекта во время беременности, могут стать:
- Краснуха. Если пациентка переболела этой болезнью на начальной стадии беременности, возрастает опасность появления у младенца врожденных пороков сердца, например, ДМПП.
- Увеличивают риск рождения ребенка с дефектом и сопутствующие заболевания у матери, например, сахарный диабет, фенилкетонурия, системная красная волчанка.
- Употребление алкоголя и прием определенных групп лекарственных препаратов (антибиотики, противоопухолевые средства).
- Контакт с фенолами, нитратами, бензпиреном.
- Ионизирующее излучение.
При ДМПП кровь проникает из левого предсердия в правое через отверстие дефекта. Кровь поступает обогащенной кислородом из легких. В правом предсердии происходит перемешивание с бедной кислородом кровью, а затем кровь вновь направляется в легкие. При дефекте большого размера легкие и правые отделы сердца испытывают чрезмерную нагрузку. С течением времени правые отделы увеличиваются, появляется гипертрофия миокарда правого предсердия и желудочка. В отдельных случаях возможен застой крови в легочном круге кровообращения и легочная гипертензия.
ДМПП отличается от незаращения овального окна, представляющего собой отверстие непатологического характера в межпредсердной перегородке, необходимое для кровотока плода в материнской утробе. После рождения ребенка отверстие чаще всего зарастает естественным образом. Если же имеет место незаращение, речь идет о ВПС.
Осложнения
Если дефект межпредсердной перегородки невелик в размерах, пациент зачастую не ощущает дискомфорта. Если же размеры дефекта большие, возможны угрожающие жизни осложнения:
- Легочная гипертензия, возникающая из-за перегрузки кровью правых сердечных отделов.
- Синдром Эйзенменгера, характеризующийся значительным ростом давления в легочной артерии. В результате давление в легочной артерии сравнивается с давлением в аорте или даже превышает его.
К прочим последствиям дефекта относят недостаточность правых сердечных отделов, аритмию, сокращенную продолжительность жизни, инсульт.
ДМПП и беременность
Если дефект межпредсердной перегородки небольшой, основная масса женщин хорошо переносит беременность. При значительном по размеру ДМПП или при наличии осложнений порока (сердечная недостаточность, нарушенный ритм сердца, легочная гипертензия), возрастает опасность осложнений у беременной женщины. При синдроме Эйзенменгера медики рекомендуют воздержаться от рождения детей, поскольку это состояние опасно для жизни женщины.
Следует учитывать и то обстоятельство, что при наличии порока у родителей вероятность возникновения ВПС у детей значительно возрастает. Поэтому при наличии факторов риска лицам, страдающим пороком сердца и желающим завести ребенка, рекомендуется пройти консультацию у врача. Также еще до беременности необходимо отказаться от приема ряда препаратов, выступающих в качестве фактора риска для возникновения дефекта.
Диагностика
Подозрения на дефект межпредсердной перегородки возникают на основании проведения аускультации, после фиксации шумов в сердце.
После аускультации назначаются следующие дополнительные методы исследований для уточнения диагноза:
- Ультразвуковая диагностика (эхокардиография). Данный диагностический метод безопасен и позволяет дать оценку функционированию сердечной мышцы, ее состоянию, а также сердечной проводимости.
- Рентгенография грудной клетки. Методика дает возможность обнаружить увеличение сердца или присутствие дополнительной жидкости в легких, что может указывать на сердечную недостаточность.
- Пульсоксиметрия. Благодаря методике можно определить содержание кислорода в крови. Для проведения исследования на кончик пальца пациента устанавливается особый датчик, регистрирующий концентрацию кислорода. Недостаточное насыщение указывает на проблемы с сердцем.
- Катетеризация. Метод состоит во введении контрастного вещества через тонкий катетер в бедренную артерию. Затем производится серия рентгеновских снимков. Методика позволяет определить состояние сердечных структур и установить величину давления в камерах сердца.
- Магнитно-резонансная томография. Благодаря МРТ можно получить картину послойного строения исследуемых тканей и органов. Преимущество метода состоит в отсутствии необходимости подвергать пациента рентгеновскому излучению. Однако методика отличается высокой стоимостью и используется в ситуациях, когда УЗИ сердца не позволяет установить точный диагноз.
Дифференциальная диагностика при ДМПП осуществляется с функциональным систолическим шумом. Шум снижается в положении стоя, правые сердечные отделы нормальной величины, нехарактерна неполная блокада правой ножки пучка Гиса. Нередко ДМПП нужно дифференцировать с такими патологиями, как триада Фалло, изолированный стеноз легочной артерии, дефект межжелудочковой перегородки, аномальный дренаж легочных вен, аномалия Эбштейна.
Лечение
Если осложнения ДМПП не создают угрозу жизни больного, в немедленном хирургическом вмешательстве нет необходимости. Срочность проведения операции также зависит от присутствия других ВПС и общего самочувствия пациента. При выявлении дефекта у ребенка медики обычно только наблюдают за его состоянием, поскольку ДМПП может зарасти самостоятельно.
Иногда дефект не закрывается самостоятельно, но отверстие настолько мало, что не создает дискомфорта человеку, и он может вести нормальную жизнь. В данной ситуации операция необязательна. Однако в большей части случаев дефект межпредсердной перегородки требует хирургического вмешательства.
Большинство специалистов рекомендует хирургическое лечение дефекта в детском возрасте. Раннее лечение позволяет избежать осложнений в зрелом возрасте. Суть операции состоит в наложении «заплаты» на дефект с тем, чтобы пресечь проникновение крови из левых сердечных отделов в правые. Хирургическое лечение предусматривает два варианта вмешательства: катетеризация и открытое хирургическое вмешательство.
Катетеризация представляет собой малоинвазивную методику, состоящую во введении по бедренной артерии тонкого зонда, конец которого доходит до ДМПП. Ход проведения операции контролируется с применением рентгеновского оборудования. С помощью зонда устанавливается специальная сетка, перекрывающая дефект. Спустя определенное время заплатка зарастает тканью, и дефект межпредсердной перегородки закрывается.
Катетеризация отличается рядом достоинств, и речь здесь идет, прежде всего, о непродолжительном периоде восстановления после операции и незначительном уровне осложнений. Также катетеризация менее травматична в сравнении с открытой хирургической операцией.
Среди потенциальных осложнений катетеризации нужно отметить следующие:
- кровотечения;
- болевой синдром;
- инфицирование в области ввода катетера;
- травмирование кровеносного сосуда;
- аллергическая реакция на контрастное вещество.
Открытое вмешательство осуществляется под общим наркозом и состоит в проведении разреза грудной клетки. Во время операции больной подключен к «искусственному сердцу». В ходе хирургического вмешательства дефект устраняется с применением «заплаты» из синтетического материала. Недостаток методики - продолжительный период восстановления пациента после операции и существенный риск развития осложнений.
Катетеризация характеризуется лучшими результатами по закрытию дефектов. Однако несколько худшая статистика по открытым операциям обусловлена, главным образом тем, что такие вмешательства назначаются в запущенных или сложных случаях.
Терапевтическое лечение ДМПП не направлено на его заращение. Однако лекарственная терапия позволяет смягчить симптоматику, а также опасность развития послеоперационных осложнений.
В числе препаратов, назначаемых пациентам, у которых выявлен дефект межпредсердной перегородки, можно назвать следующие:
- регуляторы сердечного ритма, включая бета-блокаторы и дигоксин;
- препараты для уменьшения свертываемости крови (антикоагулянты).
При первичном ДМПП осуществляются профилактические мероприятия по предотвращению эндокардита. При вторичном дефекте межпредсердной перегородки и дефектах в венозном синусе профилактика эндокардита не проводится.
Послеоперационный период и прогноз
После перенесенного хирургического вмешательства детям необходимо пожизненное наблюдение у врача. Помимо контроля за общим состоянием, проводятся исследования сердца. Важна профилактика присоединения всевозможных инфекций из-за ослабления иммунной системы после хирургического вмешательства. Поэтому рекомендуется проведение иммунизации, в частности, вакцинации против гриппа и других инфекций.
Систолический шум на верхушке сердца Остановка сердца причины
Дефект межпредсердной перегородки (сокращенно ДМПП ) — один из разновидностей врожденной патологии сердца. Он заключается в присутствии отверстия между правым и левым предсердием. ЕслиДМПП небольшой, есть шанс, что он закроется самостоятельно в первые годы жизни. Но если отверстие крупное, оно не исчезнет без операционного вмешательства. Приблизительно 7-12% новорожденных имеют ДМПП , которое может сочетаться и с другими болезнями сердечно-сосудистой системы, иногда симптомы обнаруживаются сразу, иногда в детском возрасте, а порой даже у взрослых.
Со временем ДМПП может привести к нарушению ритма, мышца сердца из-за особенностей работы истончается, возникает опасность образования тромбов, которые могут привести к инфарктам и инсультам. Исходя из всего вышесказанного, устранение ДМПП является обязательной мерой для ребенка с пороком сердца, ведь по статистике люди с отверстием между правым и левым предсердием в лучшем случае доживают до 40-50 лет.

У новорожденных ДМПП никак не проявляется, поэтому порок часто обнаруживается либо при плановой диагностике, либо при появлении специфических симптомов. ДМПП характеризуется:

Внимание: если у вашего ребенка обнаружен хотя бы один из вышеуказанных симптомов, необходимо срочно отправиться к врачу на прием. Потому как одышка, утомляемость, отеки и ускоренное сердцебиение свидетельствуют в первую очередь о наличии осложнения ДТПП (сердечной недостаточности и других характерных заболеваний).
Причины ДМПП у детей

До этого момента точные причины формирования порока сердца, в том числе ДМПП , не установлены. Если говорить о механизме возникновения патологий, то все они являются следствием нарушений развития плода на ранних этапах. Причинами называются генетические сбои и экологические факторы.

Врачи акцентируют внимание на том, что, ДМПП и другие патологии возникают как следствие негативного влияния внешнего или внутреннего характера. Течение ДМПП у детей обусловлено тем, что миокард левых отделов испытывает нагрузку меньше, чем правые, соответственно, обогащенная кровь в правом предсердии смешивается с кровью, которая практически не содержит кислорода. Поскольку она затем снова попадает в легкие, возникает перегрузка, от которой страдают правые отделы сердечной мышцы и легкие.

Со временем из-за постоянных и значительных нагрузок, правые отделы расширяются, возникает гипертрофия, а это приводит к ослаблению сердечной мышцы, о котором мы упоминали выше. Одним из осложнений на данном этапе ДМПП может стать застой жидкости в легочном круге кровообращения.
Видео — ДМПП или дефект межпредсердной перегородки
ДМПП и незаращение овального окна: различаем патологии
Когда мы говорим о ДМПП , подразумеваем наличие отверстия между правым и левым предсердием, которое анатомически не заложено; овальное окно, наоборот, является естественным отверстием, предназначающимся для осуществления кровотока плода в утробе матери. После появления ребенка на свет, овальное окно должно зарасти. Если этого не случилось, мы говорим о малой патологии (МАРС-синдром), проявления которой напрямую зависят от размеров окна. К тому же окно может закрыться на протяжении первых пяти лет жизни.

Факторы риска развития ДМПП
Как мы уже говорили ранее, врачи не могут назвать точных причин формирования пороков сердца. Однако исследования продолжают проводиться и медикам удалось обозначить факторы риска, которые при определенных условиях приводят к возникновению патологии.
Во-первых, это генетическая предрасположенность, если у кого-то из родственников поставили диагноз ДМПП , значит, у вас отягощенная наследственность. Желательно пройти консультацию у врача генетика, чтобы узнать риск возникновения этого заболевания у будущего ребенка.

Во-вторых, факторами риска являются болезни, которыми женщина переболела в процессе вынашивания плода. Например, краснуха — вирусное заболевание, особенно опасное для плода на ранних сроках беременности.

Именно в этот период формируются основные органы и возможны аномалии, например, ДМПП .
В-третьих, на развитии ребенка в утробе матери может сказаться прием некоторых медикаментозных препаратов, курение, употреблением алкоголя и плохая экологическая ситуация, стрессы, неправильное питание.

Основные осложнения ДМПП
Если отверстие маленькое, ребенок может не ощущать дискомфорта, к тому же небольшие дефекты могут закрыться сами в первые года жизни. Но если речь идет о значительном отверстии, то вскоре появляются первые осложнения. Чаще всего больным ДМПП ставят диагноз легочной гипертензии (из-за чрезмерной нагрузки правые отделы растягиваются, ослабевают и увеличиваются в размерах), возникают застойные явления.

В исключительных случаях гипертензия способствует развитию синдрома Эйзенменгера (необратимые изменения в легких).

Среди осложнений встречается аритмия, при длительном отсутствии лечения развивается сердечная недостаточность.
Диагностика сердечных патологий
Дефект перегородки можно обнаружить и в процессе планового медосмотра. Как правило, первые подозрения на ДМПП возникают после проведения аускультации (слышны шумы в сердце). Дает возможность обнаружить патологию и УЗИ сердца (эхокардиограмма).

Если ваш лечащий врач подозревает вышеуказанное отклонение в функционировании сердца, чтобы подтвердить диагноз понадобятся специфические методы исследования:
- уже указанная выше эхокардиограмма (оценивает работу сердечной мышцы и ее состояние);
- рентгенография грудной клетки (дает возможность обнаружить расширение отдельных отделов. Если на снимке видно расширение правых отделов, скорее всего, у пациента присутствует патология ДМПП );
- пульсоксиметрия (метод изучения крови на предмет содержания кислорода. Процедура абсолютно безболезненна для ребенка, выполняется с помощью датчика, он и подсчитывает количество кислорода);
- катетеризация сердца (через артерию с помощью катетера в систему кровотока впрыскивается контрастное вещество, с помощью снимков фиксируется его путь. Это позволяет сделать выводы о функциональном состоянии сердца и выявить патологию);
- МРТ (магнитно-резонансная томография) дает возможность оценить состояние структурных элементов сердца, не подвергая ребенка рентгеновскому излучению. Обычно, МРТ используют как дополнительный метод постановления диагноза, если результаты предыдущих исследований не дали однозначного ответа о наличии патологии.


Лечение ДМПП у детей
Детям с отверстием в межпредсердной перегородке нужно оперативное хирургическое вмешательство. Если отверстие небольшое, врач может принять решение какое-то время понаблюдать за состоянием ребенка. Бывает, что патология не наносит ощутимого вреда и сердце функционирует нормально. Но в большинстве случаев, наличие отверстия несет прямую угрозу жизни и операции не избежать. Риски хирургического вмешательства зависят от состояния здоровья пациента, присутствия функциональных патологий, состояния сердечной мышцы.

Медикаментозная поддержка
Ни один существующий препарат не может стимулировать устранение патологии.
Консервативное лечение направлено прежде всего на то, чтобы уменьшить негативные влияния порока и устранить риск ухудшения состояния. Больным назначают препараты, способные регулировать ритм сердца, а также антикоагулянты, чтобы предупредить образование тромбов. Медикаментозная терапия проводится также перед операцией, чтобы скорректировать состояние больного.
Оперативное вмешательство
Желательно провести операцию по устранению ДМПП сразу после его обнаружения, когда организм еще не так сильно пострадал от патологии. Операция предусматривает закрытие отверстия с помощью «заплатки» или его сшивание. Благодаря этому, удается предотвратить смешение жидкости в правом предсердии. Операция проводится путем катетеризации или на открытом сердце (пациента подключают к аппарату искусственного кровообращения и вшивают заплатку на основе синтетических не аллергенных материалов). Второй вариант операционного вмешательства опаснее из-за риска возникновения осложнений.
Эндоваскулярное закрытие патологии


Поскольку операции на открытом сердце очень опасны, требуют подключения больного к аппаратам поддержания жизни и чреваты последствиями или, как минимум, длительной реабилитацией, медики активно искали менее опасный и травматичный метод устранения пороков сердца. Когда речь идет оДМПП , операция проводится с помощью окклюдера . Это аппарат, который в сложенном виде помещается в тонкую трубку катетера и вводится пациенту. Визуально окклюдер похож на два диска, обладает эффектом памяти формы. создаются из нитинола, полностью биосовместимые , не вызывают аллергии и не обладают магнитными свойствами.

Перед операцией пациент должен пройти процедуру ультразвукового исследования сердца (транспищеводную), благодаря ей врачи получают точную информацию об особенностях строения органа и анатомии порока.

Этот метод исследования позволяет определить показания и противопоказания такого типа лечения. Несмотря на то, что эндоваскулярная операция не требует надрезов, большинству пациентов процедуру делают под наркозом (датчик вызывает дискомфорт). Информацию о размере дефекта измеряют через ЭхоКГ, затем через бедренную вену водят окклюдер (в сложенном виде) и устанавливают так, чтобы диски находились в правом и левом предсердии. Если операция успешна, заплатка закрывает просвет и кровь больше не смешивается.
Если окклюдер сместился, его втягивают в катетер и процесс повторяется. После того как заплатка установлена, аппарат извлекается наружу. Процедура занимает не более часа (с подготовкой пациента). Еще сутки пациент должен пребывать под наблюдением врачей и пройти обследование.

По статистике приблизительно 90% больных с дефектом межпредсердной перегородки могут пройти лечение таким образом. Противопоказаниями к процедуре являются дефекты без краев, а также наличие некоторых сердечно-сосудистых аномалий (принимать решение о возможности проведения эндоваскулярной операции должен врач).

Реабилитационный курс, как правило, занимает шесть месяцев. В это время пациенту стоит воздержаться от физических нагрузок, вакцинации и беременности. А также принимать ряд препаратов по предписанию доктора.
Если размер дефекта не превышает 1,2 (по некоторым данным до 3) сантиметра, его ушивают. Если отверстие больше, то оно закрывается с помощью заплатки. Второй вариант устранения патологии предпочтительнее, потому что он в меньшей степени способствует образованию тромбов на месте хирургического вмешательства.

В дальнейшем пациент должен регулярно наблюдаться у кардиохирурга, восстановительная терапия длится год. Только по прошествии этого времени больному разрешается физическая активность.
Видео — Пластика дефекта межпредсердной перегородки
Прогноз
Прогноз зависит прежде всего от того, когда была проведена операция. Если дефект был устранен в детстве или юности, есть хорошие шансы, что осложнений удастся избежать. Имеет значение и функциональное состояние сердечной мышцы: насколько на ее работу повлияла патология и какой ущерб нанесен. Чаще других среди постоперационных осложнений встречается аритмия. Если на момент операции у ребенка развилась сердечная недостаточность, устранить заболевание, увы, невозможно даже с помощью операции. В таком случае хирургическое вмешательство нужно прежде всего для того, чтобы не допустить ухудшения состояния больного. При своевременном лечении ребенок может полностью излечиться от ДМПП .

Дата публикации статьи: 15.05.2017
Дата обновления статьи: 21.12.2018
Из этой статьи вы узнаете: что такое дефект межпредсердной перегородки, почему он возникает, к каким осложнениям может привести. Как выявляют и лечат этот врожденный .
Дефект межпредсердной перегородки (сокращенно ДМПП) – это один из самых частых врожденных пороков сердца, при котором в перегородке, разделяющей правое и левое предсердие, существует отверстие. При этом пороке из левого предсердия кровь, обогащенная кислородом, попадает напрямую в правое предсердие.
В зависимости от размеров отверстия и существования других пороков, эта патология может или не иметь никаких негативных последствий, или приводить к перегрузке правых отделов сердца, и нарушениям сердечного ритма.
Открытое отверстие в межпредсердной перегородке присутствует у всех новорожденных детей, так как оно необходимо для кровообращения у плода во время внутриутробного развития. Сразу же после родов отверстие закрывается у 75% детей, однако у 25% взрослых оно остается открытым.
Пациенты с наличием данной патологии могут не иметь никаких симптомов в детском возрасте, хотя время их появления зависит от величины отверстия. Клиническая картина в большинстве случаев начинает проявляться с увеличением возраста. В возрасте 40 лет 90% людей с этим пороком, которым не проводилось лечение, страдают от одышки при физической нагрузке, усталости, сердцебиения, нарушений сердечного ритма и сердечной недостаточности.
Занимаются проблемой дефекта в межпредсердной перегородке педиатры, кардиологи и кардиохирурги.
Причины патологии
Межпредсердная перегородка (МПП) разделяет левое и правое предсердия. Во время внутриутробного развития в ней есть отверстие, называемое овальным окном, которое позволяет крови переходить из малого круга в большой, минуя легкие. Так как плод в это время получает все питательные вещества и кислород через плаценту от матери – малый круг кровообращения, основная задача которого состоит в обогащении крови кислородом в легких во время дыхания, ему не нужен. Сразу же после рождения, когда ребенок делает свой первый вдох и расправляет легкие, это отверстие закрывается. Однако так случается не у всех детей. У 25% взрослых наблюдается незакрытое овальное окно.
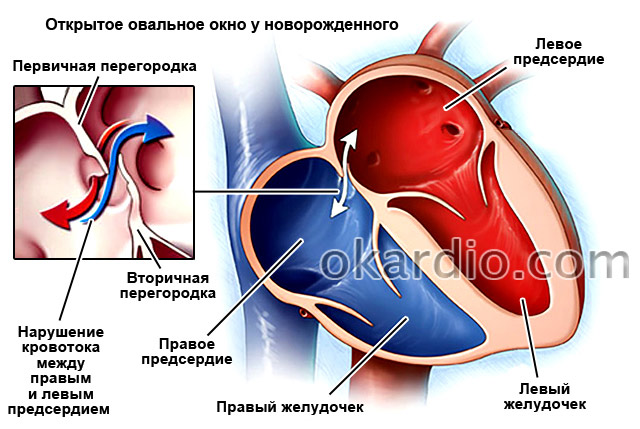
Дефект может появляться во время внутриутробного развития плода и в других частях МПП. У некоторых пациентов его возникновение может быть связано со следующими генетическими заболеваниями:
Однако у большинства пациентов причину появления ДМПП выяснить не удается.
Прогрессирование болезни
У здоровых людей уровень давления в левой половине сердца значительно выше, чем в правой, поскольку левый желудочек прокачивает кровь по всему организму, тогда как правый – лишь через легкие.
При наличии большого отверстия в МПП кровь из левого предсердия сбрасывается в правое – возникает так называемый шунт, или сброс крови слева направо. Этот дополнительный объем крови приводит к перегрузке правых отделов сердца. Без лечения это состояние может вызвать увеличение их размеров и привести к сердечной недостаточности.
Любой процесс, который повышает давление в левом желудочке, может усилить сброс крови слева направо. Это может быть артериальная гипертензия, при которой увеличивается артериальное давление, или ишемическая болезнь сердца, при которой повышается жесткость сердечной мышцы и снижается ее эластичность. Именно поэтому клиническая картина дефекта МПП развивается у людей старшего возраста, а у детей чаще всего эта патология протекает бессимптомно. Усиление шунта крови слева направо повышает давление в правых отделах сердца. Их постоянная перегрузка вызывает увеличение давления в легочной артерии, которое приводит к еще большей перегрузке правого желудочка.
Этот замкнутый круг, если его не разорвать, может привести к тому, что давление в правых отделах превысит давление в левой половине сердца. Это становится причиной возникновения сброса справа налево, при котором в большой круг кровообращения попадает венозная кровь, которая содержит небольшое количество кислорода. Появление шунта справа налево называют синдромом Эйзенменгера, это считается неблагоприятным прогностическим фактором.
Харктерные симптомы
Размер и расположение отверстия в МПП влияет на симптомы этого заболевания. Большинство детей с ДМПП выглядят полностью здоровыми и не имеют никаких признаков болезни. Они нормально растут и набирают вес. Но большой дефект межпредсердной перегородки у детей может привести к появлению следующих симптомов:
- плохой аппетит;
- плохой рост;
- усталость;
- одышка;
- проблемы с легкими – например, пневмония.

Дефекты средних размеров могут не вызывать никаких симптомов, пока пациент не вырастет и не достигнет среднего возраста. Затем могут появиться следующие признаки:
- одышка, особенно во время физической нагрузки;
- частые инфекционные заболевания верхних дыхательных путей и легких;
- ощущение сердцебиения.
Если дефект МПП не лечить, в дальнейшем у пациента могут появиться серьезные проблемы со здоровьем, включая нарушения сердечного ритма и ухудшение сократительной функции сердца. По мере взросления детей с этим заболеванием у них может повышаться риск развития инсульта, так как тромбы, которые образуются в венах большого круга кровообращения, могут проходить через отверстие в перегородке из правого предсердия в левое и попадать в мозг.
Также со временем у взрослых пациентов с нелеченым большим дефектом в МПП может развиться легочная гипертензия и синдром Эйзенменгера, проявляющиеся:
- Одышкой, которая сперва наблюдается при физической нагрузке, а со временем и в состоянии покоя.
- Усталостью.
- Головокружениями и обмороками.
- Болью или ощущением сдавливания в грудной клетке.
- Отеками на ногах, асцитом (накопление жидкости в брюшной полости).
- Синеватым цветом губ и кожи (цианоз).
У большинства детей с дефектом МПП болезнь обнаруживают и лечат задолго до того, как возникают симптомы. Из-за осложнений, возникающих во взрослом возрасте, детские кардиологи часто рекомендуют закрывать это отверстие в раннем детстве.
Диагностика
Дефект в межпредсердной перегородке может быть обнаружен во время внутриутробного развития или после рождения, а иногда и в зрелом возрасте.
Во время беременности проводятся специальные скрининговые обследования, целью которых является раннее обнаружение различных пороков развития и заболеваний. Наличие дефекта в МПП можно выявить с помощью ультразвукового исследования, создающего изображение плода.
 Ультразвуковое исследование сердца плода
Ультразвуковое исследование сердца плода
После рождения ребенка обычно педиатр при осмотре обнаруживает сердечный шум, вызванный током крови через отверстие в МПП. Наличие этого заболевания не всегда удается выявить в раннем возрасте, как другие врожденные пороки сердца (например, дефект в перегородке, разделяющей правый и левый желудочек). Вызванный патологией шум – тихий, его услышать труднее, чем другие виды сердечных шумов, из-за чего это заболевание может быть выявлено в подростковом возрасте, а иногда и позже.
Если врач слышит и подозревает наличие врожденного порока, ребенка направляют к детскому кардиологу – врачу, который специализируется на диагностике и лечении детских сердечных заболеваний. При подозрении на дефект в межпредсердной перегородке он может назначить дополнительные методы обследования, включая:
- Эхокардиографию – обследование, состоящее в получении изображения структур сердца в режиме реального времени с помощью ультразвука. Эхокардиография может показать направление кровотока через отверстие в МПП и измерить его диаметр, а также оценить, сколько крови через него проходит.
- Рентгенографию органов грудной полости – это диагностический метод, использующий рентгеновские лучи для получения изображения сердца. Если у ребенка есть дефект в МПП, сердце может быть увеличено в размерах, так как правые отделы сердца вынуждены справляться с увеличенным количеством крови. Вследствие легочной гипертензии развиваются изменения в легких, которые можно обнаружить с помощью рентгенографии.
- Электрокардиография (ЭКГ) – запись электрической активности сердца, с помощью которой можно обнаружить нарушения сердечного ритма и признаки увеличенной нагрузки на его правые отделы.
- Катетеризация сердца – это инвазивный метод обследования, дающий очень детальную информацию о внутреннем строении сердца. Через кровеносный сосуд в паху или на предплечье заводится тонкий и гибкий катетер, который осторожно направляется внутрь сердца. Во всех сердечных камерах, аорте и легочной артерии измеряется давление. Для получения четкого изображения структур внутри сердца внутрь него вводится контрастное вещество. Хотя иногда достаточное количество диагностической информации можно получить с помощью эхокардиографии, во время катетеризации сердца можно закрыть дефект МПП с помощью специального устройства.
 Методы диагностики дефекта межпредсердной перегородки
Методы диагностики дефекта межпредсердной перегородки
Методы лечения
После выявления дефекта МПП выбор метода лечения зависит от возраста ребенка, размеров и расположения отверстия, тяжести клинической картины. У детей с очень маленьким отверстием оно может закрыться самостоятельно. Более крупные дефекты сами обычно не закрываются, поэтому их нужно лечить. Большинство из них можно устранить малоинвазивным путем, хотя при некоторых ДМПП необходимо проведение открытой операции на сердце.
Ребенку с небольшим отверстием в МПП, которое не вызывает никаких симптомов, может понадобиться только регулярно посещать детского кардиолога, чтобы убедиться в том, что не появилось никаких проблем. Часто эти маленькие дефекты закрываются сами по себе, без проведения какого-либо лечения, в течение первого года жизни. Обычно у детей с маленькими дефектами в МПП нет никаких ограничений в физической активности.
Если в течение года отверстие в МПП не закрылось само, врачам часто приходится устранять его до достижения ребенком школьного возраста. Это проводится тогда, когда дефект имеет крупные размеры, сердце увеличено в размерах или появились симптомы болезни.
Малоинвазивное эндоваскулярное лечение
До начала 1990-х годов открытые операции на сердце были единственным методом закрытия всех дефектов МПП. Сегодня, благодаря достижениям медицинских технологий, врачи для закрытия некоторых отверстий в МПП используют эндоваскулярные процедуры.
Во время такой малоинвазивной операции врач вводит тонкий и гибкий катетер в вену в паху и направляет его в сердце. Этот катетер содержит подобное зонту устройство в сложенном состоянии, которое называют окклюдером. Когда катетер достигает МПП, окклюдер выталкивают из катетера и закрывают им отверстие между предсердиями. Устройство закрепляют на месте, а катетер извлекают из тела. В течение 6 месяцев над окклюдером растет нормальная ткань.

Для точного направления катетера к отверстию врачи используют эхокардиографию или ангиографию.
Эндоваскулярное закрытие дефекта МПП намного легче переносится пациентами, чем открытые операции на сердце, поскольку для их проведения необходима лишь пункция кожи в месте введения катетера. Благодаря этому облегчается восстановления после вмешательства.
Прогноз после такого лечения прекрасен, оно успешно у 90% пациентов.
Открытые операции на сердце
Иногда дефект в МПП невозможно закрыть эндоваскулярным методом, в таких случаях проводят открытые операции на сердце.
Во время хирургического вмешательства кардиохирург делает большой разрез в грудной клетке, достигает сердца и ушивает отверстие. Во время операции пациент находится в условиях искусственного кровообращения.
Прогноз при открытых операциях на сердце по закрытию дефекта МПП прекрасен, осложнения развиваются очень редко. Пациент проводит в лечебном учреждении несколько дней, затем выписывается домой.
Послеоперационный период
После закрытия дефекта в МПП пациенты наблюдаются кардиологом. Медикаментозная терапия им нужна редко. Врач может проводить наблюдение с помощью эхокардиографии и ЭКГ.
После открытой операции на сердце основное внимание уделяется заживлению разреза грудной клетки. Чем моложе пациент, тем быстрее и легче проходит процесс восстановления. Если у больного появились одышка, повышенная температура тела, покраснение около послеоперационной раны или выделения из нее, следует немедленно обратиться за медицинской помощью.
Пациентам, которым проводилось эндоваскулярное лечение ДМПП, нельзя посещать спортзал или выполнять какие-то физические упражнения в течение недели. Спустя это время они могут вернуться к своему обычному уровню активности, проконсультировавшись перед этим с врачом.
Обычно дети после операции восстанавливаются очень быстро. Но и у них могут возникать осложнения. Немедленно обратиться за медицинской помощью следует в случае появления следующих симптомов:
- Одышка.
- Синий цвет кожи на губах.
- Ухудшение аппетита.
- Отсутствие увеличения веса или его снижение.
- Сниженный уровень активности у ребенка.
- Длительное повышение температуры тела.
- Выделения из послеоперационной раны.
Прогноз
У новорожденных небольшой дефект межпредсердной перегородки часто не вызывает никаких проблем, иногда закрывается без какого-либо лечения. Большие отверстия в МПП часто требуют эндоваскулярного или хирургического лечения.
Важными факторами, влияющими на прогноз, являются размер и расположение дефекта, величина кровотока через него, наличие симптомов болезни.
При своевременном проведении эндоваскулярного или хирургического закрытия дефекта прогноз прекрасный. Если этого не сделать, у людей с большим отверстием в МПП повышается риск развития:
- нарушений сердечного ритма;
- сердечной недостаточности;
- легочной гипертензии;
- ишемического инсульта.
Представляет собой патологическое соустье между правым и левым предсердием. Он составляет около 20 % от всех врожденных пороков сердца. Дефект может располагаться в различных отделах перегородки, иметь различную форму и размеры. Условно различают первичные и вторичные (высокие) дефекты межпредсердной перегородки. Первичный дефект (рис. 5) возникает вследствие недоразвития в эмбриогенезе первичной перегородки. Отличительной его особенностью является локализация - на уровне фиброзного кольца атриовентрикулярных клапанов. Нижней стенкой такого дефекта являются фиброзные кольца митрального и трикуспидального клапанов. Дефект иногда сочетается с расщеплением митрального или тркуспидального клапанов, является компонентом так называемого открытого атриовентрикулярного канала. Вторичный дефект формируется вследствие нарушений эмбриогенеза вторичной перегородки. Нижний край такого дефекта составляет межпредсердная перегородка (рис. 5).
Гемодинамическая сущность порока заключается в сбросе артериальной крови из левого предсердия в правое и перемешивании с венозной, что вызывает гиперволемию малого круга кровообращения, а в дальнейшем – развитие легочной гипертензии. Легочная гипертензия при дефекте межпредсердной перегородки носит весьма злокачественный характер, так как необратимые изменения в легких развиваются быстро и рано, приводя к тяжелой декомпенсации правого сердца. Частым осложнением такого порока является септический эндокардит.
Клиническая картина и диагностика. Обычно жалобы связаны с декомпенсацией кровообращения. Тяжесть ее зависит от выраженности перегрузки правых отделов и развития легочной гипертензии. Больные жалуются на быструю утомляемость, одышку, легкую подверженность простудным заболеваниям, особенно в раннем детском возрасте. Аускультативно дефект межпредсердной перегородки проявляется нежным систолическим шумом с эпицентром над легочной артерией. Шум обусловлен относительным стенозом основания легочного ствола, через который протекает избыточный объем крови. Второй тон над легочной артерией усилен и часто расщеплен. На ЭКГ имеются признаки перегрузки правых отделов сердца с гипертрофией правого желудочка и предсердия. Весьма часто обнаруживается неполная или полная блокада правой ножки пучка Гиса.
При рентгенологическом исследовании определяется увеличение сердца за счет правого предсердия, желудочка и ствола легочной артерии. Имеются также повышенная пульсация корней легких и усиление общего сосудистого рисунка легочной ткани.
С помощью эхокардиографического исследования возможно визуализировать дефект межпредсердной перегородки, уточнить его характер (первичный или вторичный), оценить направление сброса через дефект (рис. 6, 7).
При зондировании сердца обнаруживается повышение давления в правом предсердии, правом желудочке и легочном стволе. Зонд может переходить из правого предсердия в левое. Контрастное вещество, введенное в левое предсердие, через дефект межпредсердной перегородки попадает в правое предсердие и далее в малый круг кровообращения. На основании рентгенологических данных можно рассчитать объем сброса крови, определить локализацию и размеры дефекта. Продолжительность жизни при дефекте межпредсердной перегородки в среднем составляет около 25 лет.
Лечение только оперативное. Преимущественно выполняют операции на открытом сердце в условиях искусственного кровообращения или гипотермии (общей или кранио-церебральной). Вторичные средней величины дефекты могут быть ушиты (рис. 8). Большие вторичные и все первичные дефекты, как правило, закрываются с использованием пластических материалов (ауто- или ксеноперикард, синтетические ткани) (рис. 9). В последнее десятилетие развивается методика транскатетерного закрытия дефекта межпредсердной перегородки при помощи «пуговичных устройств». Суть метода заключается в доставке и установке в область дефекта под рентгеновским контролем специальными инструментами-зондами двух конструкций-дисков, напоминающих пуговицы. Причем, одна из конструкций (так называемый контр-окклюдер) устанавливается со стороны правого, а другая (окклюдер) – из левого предсердия. Конструкции соединяются между собой в области дефекта при помощи специальной нейлоновой петли и перекрывают сообщение между предсердиями.
Хорошие результаты операции могут быть получены лишь при выполнении ее в раннем детском возрасте. Выполнение операции в более поздние сроки не позволяет добиться всесторонней реабилитации пациентов вследствие формирования вторичных морфологических изменений в легких, миокарде и печени. Более того, развитие легочной гипертензии со сбросом справа-налево является противопоказанием к оперативному лечению.
